با شیمی – ژوزف لویی گیلوساک
مهر 5, 1403
ارسال شده توسط ADMIN
شیمیدان فرانسوی ژوزف لویی گیلوساک (۱۷۷۸–۱۸۵۰) و دیگر دانشمندان در اواخر سده ۱۸ و اوایل قرن ۱۹ در رابطه با انبساط حرارتی گازها و رابطه بین دما و حجم و فشار گفته میشود.
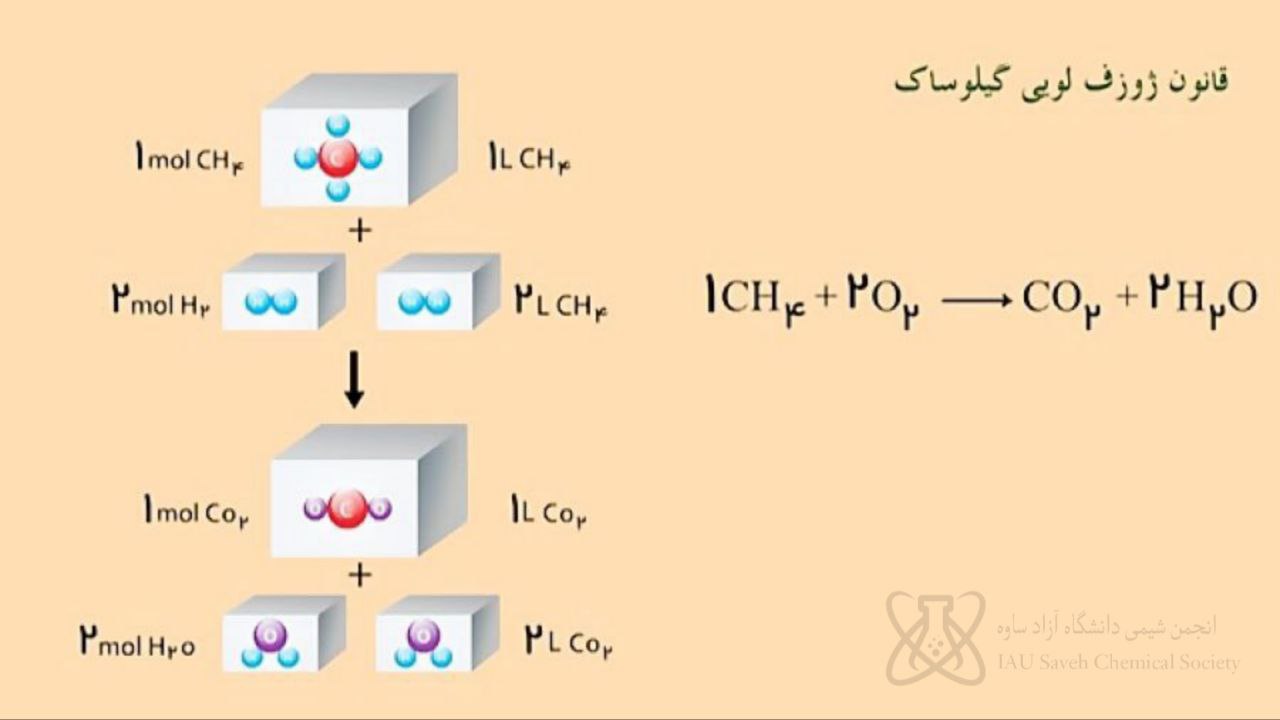
رابطه بین حجم و دما برای دو نمونه گاز مختلف که طبق قانون چارلز که توسط جوزف لوئیس گیلوساک (1802) تعیین شده است. حجم ها در 0ºC و 100ºC اندازه گیری می شوند. افزایش متناسب حجم برای همه گازها یکسان است و همه خطوط محور x را در یک نقطه قطع می کنند.
او اغلب برای قانون فشار شناخته شدهاست که میگوید فشار گاز محصور بهطور مستقیم متناسب با درجه حرارت آن است و اولین بار گیلوساک آن را تدوین و فرموله کرد (حدود سال 1808)
P=kT P1/T1=P2/T2
برچسب ها:
شیمی







دیدگاهتان را بنویسید
برای نوشتن دیدگاه باید وارد بشوید.